使い捨て腹腔鏡リニアカッターステープラーとコンポーネント パート4
(本製品を設置・使用する前に取扱説明書をよくお読みください)
Ⅷ.腹腔鏡下リニアカットステープラーメンテナンスとメンテナンス方法:
1. 保管:相対湿度80%以下、換気の良い、腐食性ガスのない室内に保管してください。
2. 輸送: 梱包された製品は通常の工具で輸送できます。輸送中は、直射日光、激しい衝突、雨、重力による押し出しを避け、慎重に取り扱ってください。
IX.腹腔鏡下リニアカットステープラー有効期限:
エチレンオキサイド滅菌後の滅菌期間は3年で、使用期限はラベルに記載されています。
X.腹腔鏡下リニアカットステープラー付属品リスト:
なし
XI に関する予防措置と警告。腹腔鏡リニア切断ステープラー:
1. この製品を使用する場合は、無菌操作仕様に厳密に従ってください。
2. 使用前に本製品のパッケージをよく確認してください。ブリスターパッケージが破損している場合は、使用を中止してください。
3. 本品はエチレンオキサイドにより滅菌処理されており、滅菌済みの医療用製品です。この製品の滅菌包装箱のディスクインジケーターを確認してください。「青」は製品が滅菌されており、臨床で直接使用できることを意味します。
4. この製品は 1 回の手術で使用されるため、使用後に滅菌することはできません。
5. 使用前に製品が有効期限内であるかどうかを確認してください。滅菌有効期間は3年間です。有効期限を過ぎた製品は固く禁止されています。
6. 当社が製造する腹腔鏡切断アセンブリは、当社が製造する対応するタイプおよび仕様の使い捨て腹腔鏡直線切断ステープラーと組み合わせて使用する必要があります。詳細については、表 1 と表 2 を参照してください。
7. 低侵襲手術は、十分な訓練を受け、低侵襲技術に精通した人が行う必要があります。低侵襲手術を行う前に、その技術、その合併症、危険性に関する医学文献を参照する必要があります。
8. 異なるメーカーの低侵襲機器のサイズは異なる場合があります。一つの手術で異なるメーカーの低侵襲手術器具や付属品を同時に使用する場合、手術前に互換性があるかどうかを確認する必要があります。
9. 手術前の放射線療法は組織変化を引き起こす可能性があります。たとえば、これらの変化により、選択されたステープルに指定されている以上に組織が肥厚する可能性があります。手術前の患者の治療は慎重に検討する必要があり、手術技術やアプローチの変更が必要になる場合があります。
10. 楽器の発射準備が整うまでボタンを放さないでください。
11. 発射前にステープル カートリッジの安全性を必ず確認してください。
12. 発射後、必ず吻合線の止血を確認し、吻合が完了したかどうか、漏れがないかどうかを確認してください。
13. 組織の厚さが指定された範囲内にあり、組織がステープラー内に均等に分布していることを確認します。片側の組織が多すぎると吻合が不十分になり、吻合部の漏出が発生する可能性があります。
14. 組織が過剰または厚い場合、トリガーを無理に引こうとすると縫合が不完全になり、吻合部の破裂や漏れが生じる可能性があります。さらに、機器の損傷や不着火が発生する可能性があります。
15. 1 つのショットを完了する必要があります。器具を部分的に点火しないでください。発射が不完全であると、ステープルの形成が不適切になったり、切断線が不完全になったり、縫合糸からの出血や漏れが発生したり、器具の取り外しが困難になったりする可能性があります。
16. ステープルが正しく形成され、組織が正しく切断されるように、必ず最後まで発射してください。
17. 発射ハンドルを握って切断刃を露出させます。ハンドルを繰り返し押さないでください。吻合部位が損傷する可能性があります。
18. 装置を挿入するときは、発射レバーが不用意に作動して、刃が偶発的に露出したり、ステープルが部分的または完全に早期に展開したりすることを避けるために、安全装置が閉じた位置にあることを確認してください。
19. 本製品の最大発射回数は8回です。
20. このデバイスを吻合線補強材とともに使用すると、ショット数が減少する可能性があります。
21. この製品は使い捨てデバイスです。一度開封したデバイスは、使用するかどうかに関わらず、再度滅菌することはできません。取り扱う前に必ず安全ロックを施錠してください。
22. 核磁気共鳴 (MR) の特定の条件下では安全:
・非臨床試験により、材料グレード TA2G の植込み型ステープルが条件付きで MR に使用できることが示されています。以下の状況では、ステープル挿入直後に患者を安全にスキャンできます。
・静磁場の範囲は1.5T〜3.0Tのみです。
・最大空間磁場勾配は3000ガウス/cm以下です。
·報告されている最大の MR システム、15 分間スキャン、全身平均吸収率 (SAR) は 2 W/kg です。
・スキャン条件下では、15分間スキャン後のステープルの最大温度上昇は1.9℃と予想されます。
アーティファクト情報:
グラディエントエコーパルスシーケンスイメージングと静磁場3.0T MRシステムを使用して非臨床テストした場合、ステープルはインプラント部位から約5 mmのところでアーチファクトを引き起こしました。
23. 製造日についてはラベルを参照してください。
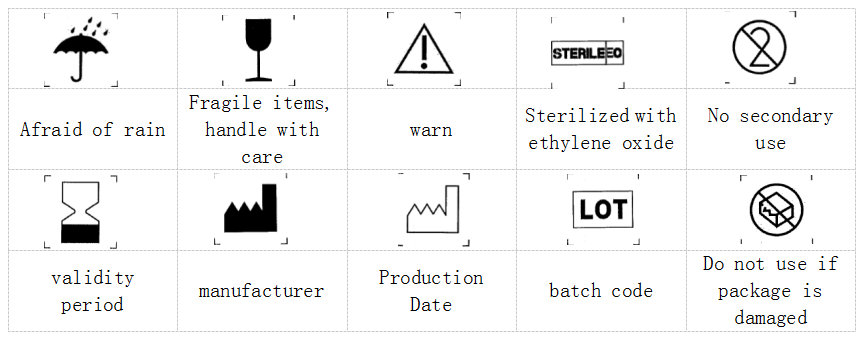
24. パッケージおよびラベルで使用されるグラフィック、記号、および略語の説明:
関連製品投稿時刻: 2023 年 1 月 20 日